Kā darbojas sienas pulkstenis, televizora tālvadības pults vai radio vadāma bērnu rotaļlieta? Lielākā daļa cilvēku bez vilcināšanās atbildēs - "no baterijām" un principā būs taisnība. Bet diez vai kāds no viņiem spēs pateikt, kā tieši pārnēsājamais akumulators ir trīskāršojies, kā tas notiek funkcijas un bez kurām būtu viss elektriskās strāvas pārnešanas process no akumulatora gala patērētājam neiespējami. Aizpildīsim šo kaitinošo zināšanu trūkumu.
Kā darbojas akumulators
Raksta saturs
- Kā darbojas akumulators
- Kā darbojas uzlādējams akumulators, tā atšķirība no parastās
Lai saprastu parastā "pirkstu" akumulatora darbības principu, ir nepieciešams vispārējs priekšstats par tā struktūru. Tātad, jebkura baterija sastāv no trim galvenajiem elementiem - anoda, katoda un elektrolīta. Turklāt pēdējam var būt praktiski jebkāds agregācijas stāvoklis: ievietots sāls šķīdumā katods un anods principā arī ir "akumulators", tikai neparasts parastajam cilvēkam uz ielas veidlapu.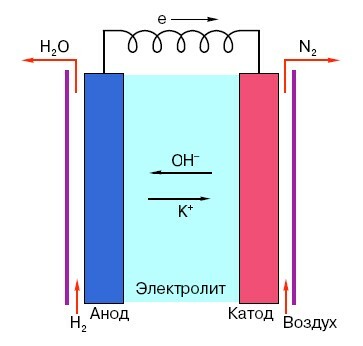
Interesanti! Tā sauktajā "voltaic pīlārā", ko izgudroja Alessandro Volta, bija arī visi elektriskās strāvas ražošanai nepieciešamie elementi. Tas sastāvēja no cinka un vara plāksnēm, kas sakrautas viena virs otras, starp kurām kā "slānis" tika ievietots skābē samērcēts audums.
Anods šādās sistēmās ir galvenais elektronu avots, kam, kā mēs zinām no skolas fizikas kursa, ir negatīvs lādiņš. Negatīvi lādētas daļiņas piesaista pozitīvās, un šajā gadījumā katoda virsma darbojas kā "plus".
Bet ar elektriskās strāvas parādīšanos ar to nepietiek, jo elektroniem ir vajadzīgs arī sava veida "šoseja" - vide, kas atbalstītu katoda un anoda mijiedarbību. Tieši šeit uz skatuves parādās elektrolīts - sāls, sārms vai skābe, kas spēj vadīt strāvu.
Analizēsim darbības principu ar konkrētu piemēru: ir akumulators, kas paredzēts 18 voltiem. Spriegums starp tajā esošajiem elektrodiem ir stabils, līdz tas tiek pievienots tīklam. Tiklīdz parādās patērētājs (piemēram, parasta spuldze), spriegums sāk pakāpeniski samazināties, sākot no "negatīvā" elektroda līdz Sāks plūst "pozitīva" strāva, un elektrolītā notiks ķīmiska reakcija, kuras mērķis ir saglabāt potenciālo atšķirību starp elektrodi.
Atsauce. Jo vairāk enerģijas patērētājam nepieciešams, jo intensīvāka reakcija plūst akumulatora iekšpusē un jo ātrāk tā neizdosies.
Kā darbojas uzlādējams akumulators, tā atšķirība no parastās
Tātad, mēs esam pārbaudījuši klasiskās "pirkstu" un "mazo pirkstu" baterijas un zinām, ka lielākās daļas to kalpošanas laiks ir stingri ierobežots (neatkarīgi no tā, ko saka izcilie ražotāji). Bet kā ir ar tā saucamajām akumulatoru baterijām - uzlādējamām baterijām, kas reakcijas laikā var ne tikai patērēt enerģiju, bet arī to uzkrāt un uzglabāt ilgu laiku?
Lai saprastu akumulatora darbības principu, ir jāvēršas pie ķīmijas. Ņemsim par piemēru... Parasts ogļu uguns. Neatkarīgi no tā, cik skaista un valdzinoša izskatās liesma, jebkurš ķīmiķis, kas to novēro, zina, ka šis process ir tikai degvielas ilgstoša oksidēšanās reakcija. Degošās ogles mijiedarbojas ar skābekli, un šīs reakcijas rezultātā mēs iegūstam:
- oglekļa dioksīds;
- gaisma;
- silti.
Un, ja pēdējie divi punkti spēj sasildīt dvēseli un ķermeni, tad mēs nekādā veidā nevaram izmantot oglekļa dioksīdu, jo tas ir reakcijas blakusprodukts, kas patiesībā ir tā atkritumi. Oksidācijas reakcija apstājas, kad beidzas sākotnējie elementi: skābeklis un ogles. Reakcijas apstāšanās akumulatorā notiek tādā pašā veidā, kad izejvielas pilnībā izplūst un paliek tikai "atkritumi".
Akumulatorā viss notiek nedaudz savādāk. Fakts ir tāds, ka reakcija, kas tajā notiek, pieder pie atgriezeniskas kategorijas, tas ir, noteiktos apstākļos to var "mainīt", atgriežot visas vielas sākotnējā stāvoklī. Tieši atgriezeniskas reakcijas iespēja akumulatorā ļauj to uzlādēt.
Tīklam pievienotajā akumulatorā reakcija notiek pretējā virzienā, un strāva plūst no "plus" uz "mīnus", nevis otrādi. Rezultātā reakcijas produkts veido sākotnējās vielas, un akumulatora īpašnieks pārnēsājamā formātā saņem pieejamo "atgūto" enerģiju. Tas ir viss!
Abonējiet mūsu sociālos tīklus


