Jak działa zegar ścienny, pilot do telewizora lub dziecięca zabawka sterowana radiem? Większość ludzi bez wahania odpowie - „z baterii” i w zasadzie będzie miała rację. Ale mało który z nich będzie w stanie powiedzieć, w jaki sposób bateria przenośna jest potrojona, jak to się dzieje funkcji i bez których byłby cały proces przesyłania prądu elektrycznego z akumulatora do odbiorcy końcowego niemożliwe. Wypełnijmy tę irytującą lukę w wiedzy.
Jak działa bateria?
Treść artykułu
- Jak działa bateria?
- Jak działa akumulator, różni się od konwencjonalnego
Aby zrozumieć zasadę działania konwencjonalnej baterii „palcowej”, konieczne jest ogólne pojęcie o jej strukturze. Tak więc każda bateria składa się z trzech głównych elementów - anody, katody i elektrolitu. Co więcej, te ostatnie mogą mieć praktycznie dowolny stan skupienia: umieszczone w roztworze soli fizjologicznej katoda i anoda w zasadzie też są „baterią”, tylko w nietypowy dla przeciętnego człowieka sposób Formularz.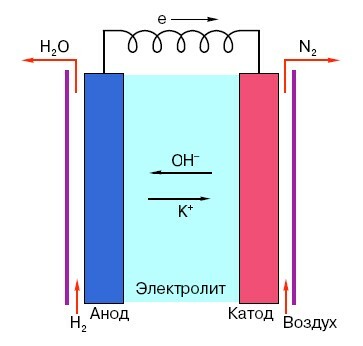
Ciekawe! Tak zwany „słup elektryczny”, wynaleziony przez Alessandro Voltę, również posiadał wszystkie elementy niezbędne do wytwarzania prądu elektrycznego. Składał się z ułożonych jedna na drugiej płyt cynkowych i miedzianych, pomiędzy którymi jako „warstwę” umieszczono tkaninę nasączoną kwasem.
Anoda w takich układach jest głównym źródłem elektronów, które, jak wiemy ze szkolnego kursu fizyki, mają ładunek ujemny. Cząstki naładowane ujemnie są przyciągane do cząstek dodatnich iw tym przypadku powierzchnia katody działa jak „plus”.
Ale do pojawienia się prądu elektrycznego to nie wystarczy, ponieważ elektrony również potrzebują swoistej „autostrady” - ośrodka, który wspierałby oddziaływanie katody i anody. To tutaj „na scenie” pojawia się elektrolit – sól, zasada lub kwas zdolny do przewodzenia prądu.
Przeanalizujmy zasadę działania na konkretnym przykładzie: istnieje bateria zaprojektowana na 18 woltów. Napięcie między elektrodami w nim jest stabilne, dopóki nie zostanie podłączone do sieci. Gdy tylko pojawi się konsument (na przykład zwykła żarówka), napięcie zaczyna stopniowo spadać, od elektrody „ujemnej” do Zacznie płynąć „dodatni” prąd, a w elektrolicie zajdzie reakcja chemiczna mająca na celu utrzymanie różnicy potencjałów między elektrody.
Odniesienie. Im więcej energii potrzebuje konsument, tym intensywniejsza reakcja przepływa wewnątrz akumulatora i tym szybciej się zawiedzie.
Jak działa akumulator, różni się od konwencjonalnego
Zbadaliśmy więc klasyczne baterie „na palec” i „mały palec” i wiemy, że żywotność większości z nich jest ściśle ograniczona (cokolwiek mówią wybitni producenci). Ale co z tzw. bateriami akumulatorowymi – akumulatorami, które mogą nie tylko zużywać energię podczas reakcji, ale także ją akumulować i przechowywać przez długi czas?
Aby zrozumieć zasadę działania baterii, należy zwrócić się do chemii. Weźmy jako przykład... Zwykły kominek na węgiel drzewny. Bez względu na to, jak pięknie i urzekająco może wyglądać płomień, każdy chemik obserwujący go wie, że proces ten jest tylko długotrwałą reakcją utleniania paliwa. Spalanie węgla oddziałuje z tlenem i w wyniku tej reakcji otrzymujemy:
- dwutlenek węgla;
- lekki;
- serdecznie.
A jeśli dwa ostatnie punkty są w stanie ogrzać duszę i ciało, to nie możemy w żaden sposób wykorzystać dwutlenku węgla, ponieważ jest to produkt uboczny reakcji, który w rzeczywistości jest jego odpadem. Reakcja utleniania kończy się wraz z wyczerpaniem się pierwiastków początkowych: tlenu i węgla. Zatrzymanie reakcji w akumulatorze następuje w ten sam sposób, gdy substancje wyjściowe całkowicie się wyczerpują i pozostają tylko „odpady”.
W akumulatorze wszystko dzieje się trochę inaczej. Faktem jest, że reakcja, która w nim zachodzi, należy do kategorii odwracalnej, to znaczy w pewnych warunkach można ją „odwrócić”, przywracając wszystkie substancje do ich pierwotnego stanu. To właśnie możliwość odwracalnej reakcji w akumulatorze umożliwia jego ładowanie.
W akumulatorze podłączonym do sieci reakcja przebiega w odwrotnym kierunku, a prąd płynie od „plusa” do „minusu”, a nie odwrotnie. W efekcie produkt reakcji tworzy substancje wyjściowe, a właściciel baterii otrzymuje dostępną „odzyskaną” energię w przenośnym formacie. To wszystko!
Subskrybuj nasze sieci społecznościowe


