Como funciona um relógio de parede, controle remoto de TV ou brinquedo de criança controlado por rádio? A maioria das pessoas, sem hesitação, responderá - "com baterias" e, em princípio, estará certa. Mas dificilmente algum deles será capaz de dizer exatamente como uma bateria portátil é triplicada, como ela funções e sem as quais todo o processo de transferência de corrente elétrica da bateria para o consumidor final seria impossível. Vamos preencher essa lacuna de conhecimento irritante.
Como funciona a bateria
O conteúdo do artigo
- Como funciona a bateria
- Como funciona uma bateria recarregável, diferente de uma convencional
Para entender o princípio de funcionamento de uma bateria convencional de "dedo", é necessário ter uma ideia geral de sua estrutura. Portanto, qualquer bateria consiste em três elementos principais - ânodo, cátodo e eletrólito. Além disso, este último pode ter virtualmente qualquer estado de agregação: colocado em solução salina o cátodo e o ânodo, em princípio, também são uma "bateria", só que de forma incomum para o homem comum na rua Formato.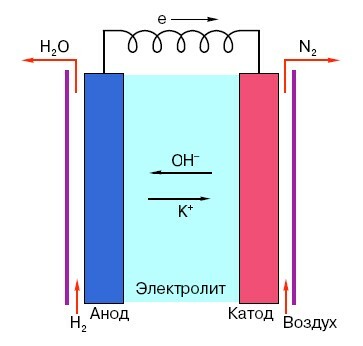
Interessante! O chamado "pilar voltaico", inventado por Alessandro Volta, também contava com todos os elementos necessários para a produção de corrente elétrica. Consistia em placas de zinco e cobre empilhadas umas sobre as outras, entre as quais um pano embebido em ácido era colocado como uma "camada".
O ânodo nesses sistemas é a principal fonte de elétrons, que, como sabemos do curso de física da escola, têm carga negativa. Partículas carregadas negativamente são atraídas pelas positivas e, neste caso, a superfície do cátodo atua como um "sinal de adição".
Mas para o surgimento de uma corrente elétrica, isso não é suficiente, porque os elétrons também precisam de uma espécie de "rodovia" - um meio que suportaria a interação do cátodo e do ânodo. É aqui que o eletrólito aparece "em cena" - sal, álcali ou ácido capaz de conduzir corrente.
Vamos analisar o princípio de funcionamento com um exemplo específico: existe uma bateria projetada para 18 volts. A tensão entre os eletrodos nele é estável até que seja conectado à rede. Assim que um consumidor aparece (por exemplo, uma lâmpada comum), a voltagem começa a diminuir gradualmente, do eletrodo "negativo" para A corrente "positiva" começará a fluir, e uma reação química ocorrerá no eletrólito, visando manter a diferença de potencial entre eletrodos.
Referência. Quanto mais energia o consumidor precisa, mais intensa a reação flui dentro da bateria e mais rápido ela falhará.
Como funciona uma bateria recarregável, diferente de uma convencional
Portanto, examinamos as baterias clássicas de "dedo" e "dedo mínimo" e sabemos que a vida útil da maioria delas é estritamente limitada (o que quer que digam os fabricantes eminentes). Mas e as chamadas baterias de acumuladores - baterias recarregáveis que podem não apenas consumir energia durante a reação, mas também acumulá-la e armazená-la por um longo tempo?
Para entender o princípio da bateria, é necessário recorrer à química. Tomemos como exemplo... Um fogo de carvão comum. Não importa o quão bela e fascinante a chama possa parecer, qualquer químico que a observe sabe que esse processo é apenas uma reação de oxidação de longo prazo do combustível. A queima de carvão interage com o oxigênio e, como resultado dessa reação, obtemos:
- dióxido de carbono;
- luz;
- calorosamente.
E se os dois últimos pontos são capazes de aquecer a alma e o corpo, então não podemos usar o dióxido de carbono de forma alguma, porque é um subproduto da reação, que é, na verdade, seu resíduo. A reação de oxidação para quando os elementos iniciais são exauridos: oxigênio e carvão. A parada da reação na bateria ocorre da mesma forma quando as substâncias de partida se exaurem completamente e apenas "resíduos" permanecem.
Na bateria, tudo acontece de maneira um pouco diferente. O fato é que a reação que nele ocorre pertence à categoria dos reversíveis, ou seja, sob certas condições pode ser "revertida", devolvendo todas as substâncias ao seu estado original. É a possibilidade de uma reação reversível na bateria que torna possível carregá-la.
Em uma bateria conectada à rede, a reação ocorre na direção oposta, e a corrente flui de "mais" para "menos", e não vice-versa. Como resultado, o produto da reação forma as substâncias iniciais, e o dono da bateria recebe a energia "recuperada" disponível em formato portátil. Isso é tudo!
Inscreva-se em nossas redes sociais